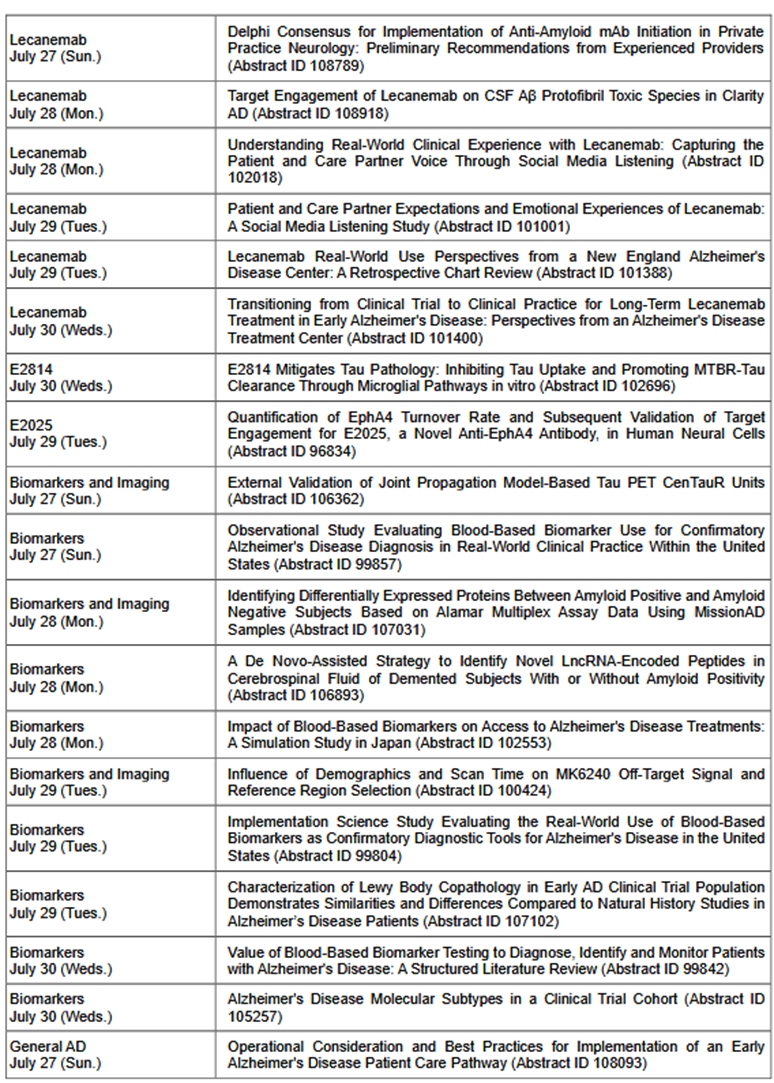
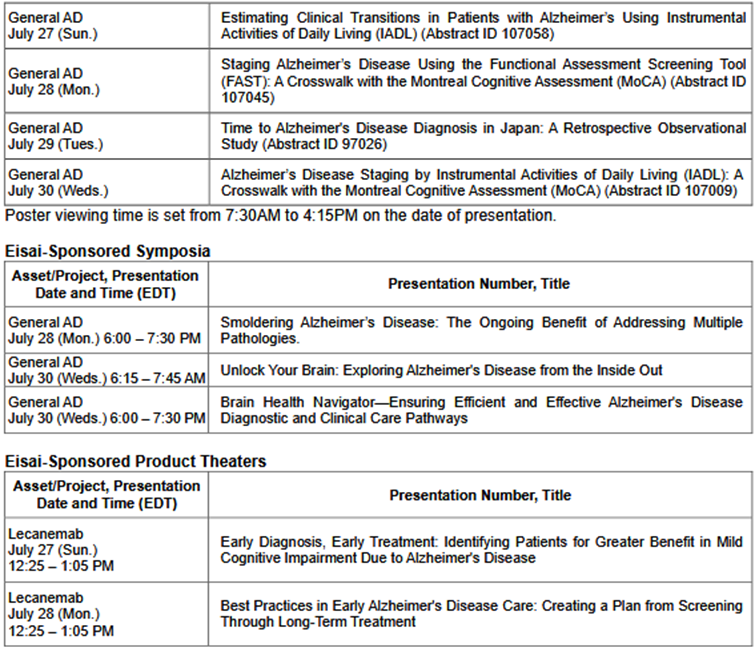
倡导全社会关注癫痫患者全程健康管理,推动诊疗服务与社会支持体系的优化,聚焦“科技+医疗+人文”融合,展示癫痫防治领域前沿技术与应用成果的转化。社会关注癫痫患者全程健康管理,推动诊疗服务与社会支持体系的优化,聚焦“科技+医疗+人文”融合,展示癫痫防治领域前沿技术与应用成果的转化。
今年6月28日是“第十九个国际癫痫关爱日”,此次宣传主题为 “科技助力,共创未来”。在“国际癫痫关爱日”来临之际,中国抗癫痫协会一如既往的向患者及公众宣传疾病相关知识并有序组织患教活动。6月21日上午9:00-12:00,由中国抗癫痫协会和广东省抗癫痫协会共同主办的“国际癫痫关爱日主会场大型公益活动”在深圳光明区光明天安云谷国际会议中心举行,卫材中国作为企业代表参与了此次活动,卫材中国药业基础治疗事业部总经理吴猛先生代表企业进行了“尽企业社会责任,造福广大癫痫患者”主题发言。

卫材中国药业总经理吴猛发表主题讲话
吴猛表示,癫痫并非不治之症,通过科学的药物治疗大部分患者都可以控制病情甚至治愈。作为一家具备研发能力的跨国制药企业,卫材中国秉承hhc(human health care,关心人类健康)的企业理念,致力于为疾病治愈提供新的药物选择。同时,卫材中国也积极投身癫痫公益事业,自2020年以来连续6年参与癫痫患者关爱日活动,我们将继续以开放协作的姿态,与各方伙伴携手并进,持续引入全球创新成果,并立足中国患者需求进行本土化深耕,让前沿科技真正转化为患者触手可及的希望与切实改善的生活品质。
癫痫,这一患病人数仅次于卒中的第二大神经系统疾病,影响着近1000万癫痫患者的生活。患者不仅面临疾病本身的挑战,更承受着社会误解、就医不便、自我管理困难等多重压力。传统的疾病管理模式,往往难以满足患者对精准、便捷、个性化诊疗支持的迫切需求。本次活动旨在搭建一个融合前沿科技、医学智慧与患者关爱的交流平台,让创新科技成为连接希望与健康的坚实桥梁。
本次活动中将重磅呈现科技如何重塑癫痫患者的健康管理图景:
智慧守护,触手可及:深入解读可穿戴智能设备(如癫痫预警手环)、移动健康APP如何实现精准监测,智能识别潜在发作风险,为患者构建全天候“电子安全网”,极大提升安全感与独立生活能力。
云端问诊,资源普及:展示远程医疗平台如何打破地域藩篱,让身处偏远地区的患者一键连接顶级癫痫专家,足不出户获取专业评估与用药指导,让优质医疗资源跨越时空阻隔。
数据驱动,精准护航:揭秘数字疗法与AI分析工具如何将患者日常记录的用药、发作、睡眠等海量数据转化为个性化管理方案,辅助医生优化治疗决策,实现从“经验医疗”到“精准医疗”的关键跃升。


6.28国际癫痫关爱日大型公益活动现场图片
本场公益活动受邀参与的嘉宾有:中国抗癫痫协会会长周东教授、广东省深圳市光明区政府党组成员王崇峰副区长、中山大区附属第七医院陈起坤党委书记、中国抗癫痫协会创会会长李世绰教授、中国抗癫痫协会癫痫病友工作委员会主委丁玎教授、中国抗癫痫协会副会长周列民教授等。
该活动引起了社会各界人士的关注并纷纷发表各自观点,共同呼吁全社会对于中国近1000万癫痫患者的关爱。近年来,随着医学科技进步及国家脑科学领域战略布局与政策支持,我国癫痫诊疗取得了突破性进展。在时代背景下,科技正为我们全面赋能,从精准诊断、个性化治疗、患者全程管理与人文关怀等多个方面,重塑癫痫防治模式,助力健康中国战略。中国抗癫痫协会将继续在全国范围内号召和组织开展多种形式的“癫痫关爱日公益活动”。继续开展不同规模和多种形式的公益和宣教活动,营造关爱癫痫患者的社会氛围。

6.28国际癫痫关爱日大型公益活动现场图片
作为一家具备研发能力的跨国制药企业,卫材中国在神经科学领域、肿瘤领域、消化肝病领域均有原研药物在华销售。其中,第三代抗癫痫发作药物吡仑帕奈于2019年9月通过优先审评,至今已服务中国癫痫患者近6年时间。2021年7月该药物通过国家药监局的评审,用于成人和4岁及以上儿童癫痫部分性发作患者(伴有或不伴有继发全面性发作)的治疗;2024年4月30日,吡仑帕奈在华新适应症获得国家药品监督管理局批准——成人和12岁及以上儿童癫痫原发性全面性强直-阵挛发作患者的加用治疗。同时,为了更好的提升患者用药的便利性,吡仑帕奈2024年在中国上市口服混悬液剂型,更加利于吞咽障碍和儿科患者的使用。另外,2020年12月卫克泰已被正式纳入中国《国家基本医疗保险、工伤保险和生育保险药品目录(2020年版)》。

6.28国际癫痫关爱日大型公益活动志愿者及与会专家现场演绎“送你一朵小红花”
最后,在志愿者及与会专家共同演绎的“送你一朵小红花”歌声中结束了本次活动,此次活动不仅为癫痫患者和家属提供了学习交流平台,也进一步推动了癫痫防治事业的发展。相信在科技的助力下,在社会各界人士的共同关注下,癫痫患者一定能够拥有更加美好的未来!